|
Se non visualizzi correttamente la newsletter Clicca qui
|

|
CLINICAL NEWS
|
Per i professionisti della sanità | N 1 | ottobre 2017
|
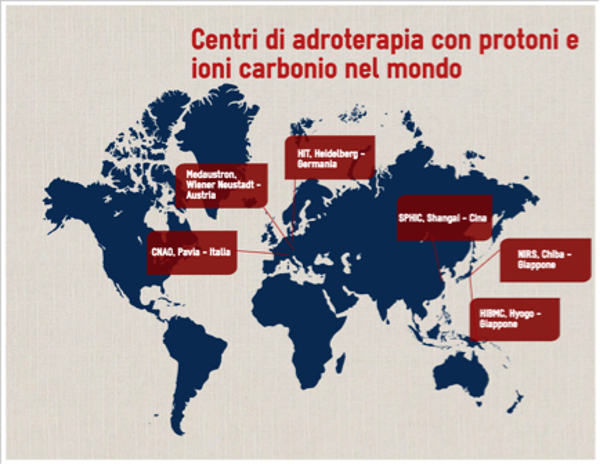 L’adroterapia in Italia entra nei LEA
Con questo primo numero della newsletter CNAO Clinical News vogliamo contribuire a migliorare la conoscenza dell’adroterapia e delle sue applicazioni cliniche. Da marzo 2017 l’adroterapia è stata ufficialmente inserita nei Livelli Essenziali d’Assistenza
Vantaggi dell’adroterapia e applicazioni cliniche attuali
L’adroterapia presenta vantaggi clinici distintivi rispetto alla radioterapia con fotoni, in termini sia di efficacia sia di tollerabilità e sicurezza. Innanzitutto, l’impiego di particelle subatomiche permette di aggredire tumori poco o per nulla danneggiati dalla radioterapia convenzionale (tumori radio-resistenti) e contro i quali non esistono altre opzioni terapeutiche soddisfacenti. A oggi, la terapia con protoni o ioni carbonio ha dimostrato di migliorare sensibilmente il controllo locale, la sopravvivenza libera da malattia (PFS) e la sopravvivenza globale (OS) in pazienti affetti da carcinomi e adenocarcinomi (in particolare, quelli localizzati a livello della testa e del collo), sarcomi, cordomi e condrosarcomi, tumori cerebrali, spinali e della base cranica, melanomi uveali ecc.
In aggiunta, grazie alle peculiari caratteristiche di rilascio profondo dell’energia di protoni e ioni carbonio (focalizzata a fine percorso nel cosiddetto come “picco di Bragg”), l’adroterapia interferisce minimamente con i tessuti sani che circondano il tumore, limitando sia reazioni infiammatorie e degenerative acute in corso di trattamento e nelle settimane successive sia disturbi e complicanze tardive, compresa l’insorgenza di tumori secondari all’irraggiamento. Queste caratteristiche rendono l’adroterapia l’approccio ideale per il controllo di tumori localizzati in prossimità di aree critiche, come l’encefalo, l’occhio, i nervi encefalici e spinali (ma anche i polmoni, il cuore, l’esofago e i vasi toracici e addominali) e per il trattamento di neoplasie pediatriche.
Al momento, le applicazioni cliniche dell’adroterapia riguardano principalmente forme tumorali “statiche”, per le quali può essere precisamente definito un campo di irraggiamento 3D con TAC e risonanza magnetica (RM) e pianificati una dose ottimale e parametri di trattamento in funzione della specifica neoplasia, del tipo e dello spessore dei tessuti che le particelle devono attraversare, nonché del loro grado di ossigenazione (fattore potenzialmente interferente). Ancora limitati a pochi centri di adroterapia tra cui il CNAO e, perlopiù, offerti nell’ambito di protocolli sperimentali sono, invece, i trattamenti indirizzati ad aggredire masse tumorali “in movimento”, ossia soggette a spostamenti più o meno ampi a causa della respirazione, del battito cardiaco o di altre funzioni fisiologiche fondamentali. Tra le neoplasie già in cura, ma non riconosciute nei LEA, vi sono i tumori del pancreas e del fegato; di questo tipo potenzialmente trattabili con adroterapia nel prossimo futuro si possono ricordare il cancro del polmone e quello della mammella, i linfomi del mediastino e i timomi,. In tutti questi casi, per riuscire a offrire trattamenti adroterapici efficaci e sicuri è necessario superare diverse criticità tecnologiche, a partire dalla messa a punto di sistemi di localizzazione dinamica del target tumorale e dei suoi rapporti con le strutture anatomiche circostanti e di pianificazione dinamica della dose di particelle da somministrare.
Le indicazioni dell’adroterapia inserite nei LEA
A oggi, Fondazione CNAO ha trattato con adroterapia oltre 1.500 pazienti italiani e stranieri. Prevedibilmente, nei prossimi mesi, il numero dei pazienti trattati sul territorio nazionale aumenterà sensibilmente, sia perché le indicazioni dell’adroterapia si stanno moltiplicando sia perché dieci tra quelle maggiormente consolidate e ritenute cruciali per i pazienti sono state inserite nei nuovi Livelli Essenziali d’Assistenza (LEA), secondo il decreto del Presidente del Consiglio dei Ministri di aggiornamento dei LEA del 12 gennaio 2017 (GU n. 65, Suppl ordinario 1S, 18 marzo 2017; http://www.gazzettaufficiale.it/eli/id/2017/03/18/17A02015/sg)
LINK ALLE PATOLOGIE RICONOSCIUTE NEI LEA:https://fondazionecnao.it/it/news-cnao/2017/180-l-adroterapia-e-entrata-nel-sistema-sanitario-nazionale
Grazie a questo decreto, tutti i pazienti oncologici adulti e pediatrici italiani interessati da queste patologie possono accedere gratuitamente al trattamento con protoni o con ioni carbonio erogati dal CNAO,in base ai protocolli attivi. Per il trattamento con adroterapia di forme tumorali non ancora inserite nei LEA, per pazienti con specifiche caratteristiche patologiche e cliniche, è inoltre possibile l’inserimento in studi clinici prospettici attivi, per altri pazienti le prestazioni sono disponibili a pagamento in attesa dell’estensione delle casistiche rientranti nei LEA.
L’adroterapia in Italia entra nei LEA
Con questo primo numero della newsletter CNAO Clinical News vogliamo contribuire a migliorare la conoscenza dell’adroterapia e delle sue applicazioni cliniche. Da marzo 2017 l’adroterapia è stata ufficialmente inserita nei Livelli Essenziali d’Assistenza
Vantaggi dell’adroterapia e applicazioni cliniche attuali
L’adroterapia presenta vantaggi clinici distintivi rispetto alla radioterapia con fotoni, in termini sia di efficacia sia di tollerabilità e sicurezza. Innanzitutto, l’impiego di particelle subatomiche permette di aggredire tumori poco o per nulla danneggiati dalla radioterapia convenzionale (tumori radio-resistenti) e contro i quali non esistono altre opzioni terapeutiche soddisfacenti. A oggi, la terapia con protoni o ioni carbonio ha dimostrato di migliorare sensibilmente il controllo locale, la sopravvivenza libera da malattia (PFS) e la sopravvivenza globale (OS) in pazienti affetti da carcinomi e adenocarcinomi (in particolare, quelli localizzati a livello della testa e del collo), sarcomi, cordomi e condrosarcomi, tumori cerebrali, spinali e della base cranica, melanomi uveali ecc.
In aggiunta, grazie alle peculiari caratteristiche di rilascio profondo dell’energia di protoni e ioni carbonio (focalizzata a fine percorso nel cosiddetto come “picco di Bragg”), l’adroterapia interferisce minimamente con i tessuti sani che circondano il tumore, limitando sia reazioni infiammatorie e degenerative acute in corso di trattamento e nelle settimane successive sia disturbi e complicanze tardive, compresa l’insorgenza di tumori secondari all’irraggiamento. Queste caratteristiche rendono l’adroterapia l’approccio ideale per il controllo di tumori localizzati in prossimità di aree critiche, come l’encefalo, l’occhio, i nervi encefalici e spinali (ma anche i polmoni, il cuore, l’esofago e i vasi toracici e addominali) e per il trattamento di neoplasie pediatriche.
Al momento, le applicazioni cliniche dell’adroterapia riguardano principalmente forme tumorali “statiche”, per le quali può essere precisamente definito un campo di irraggiamento 3D con TAC e risonanza magnetica (RM) e pianificati una dose ottimale e parametri di trattamento in funzione della specifica neoplasia, del tipo e dello spessore dei tessuti che le particelle devono attraversare, nonché del loro grado di ossigenazione (fattore potenzialmente interferente). Ancora limitati a pochi centri di adroterapia tra cui il CNAO e, perlopiù, offerti nell’ambito di protocolli sperimentali sono, invece, i trattamenti indirizzati ad aggredire masse tumorali “in movimento”, ossia soggette a spostamenti più o meno ampi a causa della respirazione, del battito cardiaco o di altre funzioni fisiologiche fondamentali. Tra le neoplasie già in cura, ma non riconosciute nei LEA, vi sono i tumori del pancreas e del fegato; di questo tipo potenzialmente trattabili con adroterapia nel prossimo futuro si possono ricordare il cancro del polmone e quello della mammella, i linfomi del mediastino e i timomi,. In tutti questi casi, per riuscire a offrire trattamenti adroterapici efficaci e sicuri è necessario superare diverse criticità tecnologiche, a partire dalla messa a punto di sistemi di localizzazione dinamica del target tumorale e dei suoi rapporti con le strutture anatomiche circostanti e di pianificazione dinamica della dose di particelle da somministrare.
Le indicazioni dell’adroterapia inserite nei LEA
A oggi, Fondazione CNAO ha trattato con adroterapia oltre 1.500 pazienti italiani e stranieri. Prevedibilmente, nei prossimi mesi, il numero dei pazienti trattati sul territorio nazionale aumenterà sensibilmente, sia perché le indicazioni dell’adroterapia si stanno moltiplicando sia perché dieci tra quelle maggiormente consolidate e ritenute cruciali per i pazienti sono state inserite nei nuovi Livelli Essenziali d’Assistenza (LEA), secondo il decreto del Presidente del Consiglio dei Ministri di aggiornamento dei LEA del 12 gennaio 2017 (GU n. 65, Suppl ordinario 1S, 18 marzo 2017; http://www.gazzettaufficiale.it/eli/id/2017/03/18/17A02015/sg)
LINK ALLE PATOLOGIE RICONOSCIUTE NEI LEA:https://fondazionecnao.it/it/news-cnao/2017/180-l-adroterapia-e-entrata-nel-sistema-sanitario-nazionale
Grazie a questo decreto, tutti i pazienti oncologici adulti e pediatrici italiani interessati da queste patologie possono accedere gratuitamente al trattamento con protoni o con ioni carbonio erogati dal CNAO,in base ai protocolli attivi. Per il trattamento con adroterapia di forme tumorali non ancora inserite nei LEA, per pazienti con specifiche caratteristiche patologiche e cliniche, è inoltre possibile l’inserimento in studi clinici prospettici attivi, per altri pazienti le prestazioni sono disponibili a pagamento in attesa dell’estensione delle casistiche rientranti nei LEA.
|
 Ioni carbonio efficaci contro i carcinomi non-squamosi del distretto testa-collo
Uno studio prospettico conferma le evidenze di efficacia e sicurezza dell’adroterapia con ioni carbonio nel controllo dei carcinomi adenoideo-cistici e di altre forme non squamose del distretto testa-collo, con esiti particolarmente favorevoli in caso di
L’adroterapia con ioni carbonio offre la possibilità di controllare la malattia e migliorare la sopravvivenza di pazienti interessati da carcinomi a cellule non squamose del distretto testa-collo, di norma resistenti alla radioterapia convenzionale con fotoni e ai regimi chemioterapici disponibili. A confermare le precedenti evidenze favorevoli in questo senso è uno studio prospettico condotto su 35 pazienti affetti principalmente da adenocarcinoma adenoideo-cistico (60% dei casi), trattati con ioni carbonio presso il GunmaUniversityHeavyIonMedical Center di Maebashi (Giappone), dopo conferma istologica della neoplasia.
Per essere inclusi nello studio, i pazienti dovevano avere un’età compresa tra 16 e 80 anni, tumore misurabile N0-1 M0 e performance status 0-2, non essere mai stati sottoposti a radioterapia a livello di testa e collo, non aver ricevuto chemioterapia nei 30 giorni precedenti l’arruolamento né presentare infezioni non controllate, tumori in altre sedi o comorbilità severe. L’adroterapia con ioni carbonio è stata somministrata al dosaggio di 64,0 Gy RBE (Relative BiologicalEffectiveness) a 32 pazienti e di 57,6 Gy RBE ai restanti tre, in 16 frazioni in entrambi i casi.
Il trattamento ha permesso di ottenere il controllo locale della malattia a tre anni nel 93% dei pazienti (end point primario dello studio) e una sopravvivenza globale (OS, OverallSurvival) a tre anni nell’88% dei casi (end point secondario), a conferma dell’efficacia degli ioni carbonio nell’aggredire e nel neutralizzare tumori altrimenti difficilmente attaccabili.
Esiti particolarmente incoraggianti sono stati ottenuti nei carcinomi non squamosi di minori dimensioni (T2, 5/35 pazienti) e nei tumori diversi dal carcinoma adenoideo-cistico (tra cui 5 neuroblastomi olfattivi, 4 carcinomi mucoepidermoidi e 2 adenocarcinomi): in entrambi i casi, il controllo locale della malattia a tre anni è stato del 100%.
La minore dimensione del tumore è risultata correlata anche all’OS a tre anni, risultata pari al 100% per i tumori T2, e alla localizzazione della neoplasia. In questo secondo caso, l’OS a tre anni è arrivata al 100% per i carcinomi presenti a livello della cavità orale, della faringe e delle parotidi, all’88% per i tumori del seno mascellare e della cavità nasale.
Ulteriori end point secondari esaminati comprendevano il tasso di sopravvivenza libera da malattia (PFS) a tre anni (risultato globalmente pari al 71% e al 100% nei pazienti con tumore T2), la qualità di vita correlata alla salute (valutata con questionario SF-8, prima e dopo 1, 3, 6, 12 e 24 mesi dall’adroterapia) e gli eventi avversi acuti e tardivi.
Relativamente a quest’ultimo aspetto, il trattamento ha comportato complicanze in una quota non trascurabile di pazienti, con sviluppo di mucosite e dermatite acute radioindotte di grado 2-3 rispettivamente nel 65% e nel 31% dei trattati e di mucosite tardiva radioindotta di grado 2 e 3 rispettivamente in 11 e in 1 pazienti.
Mucosite e dermatite acute sono rapidamente migliorate con terapia conservativa e non sembrano costituire una criticità rilevate. Per ridurre l’incidenza di eventi avversi tardivi si ritiene indispensabile prevedere un’attenta pianificazione iniziale della dose nell’ottica di limitare il disagio per il paziente e tutelarne la qualità di vita, senza inficiare l’efficacia del trattamento con ioni carbonio.
Il tasso di tossicità G3 sia acuta che tardiva rilevata nel seguente studio è nettamente inferiore a quanto segnalato in trattamenti convenzionali (tossicità G3/4 mucosa e cutanea intorno al 50%).
Reference
Shirai K et al. Prospective observational study of carbon-ion radiotherapy for non-squamous cell carcinoma of the head and neck. Cancer Sci 2017; doi:10.1111/cas.13325
Ioni carbonio efficaci contro i carcinomi non-squamosi del distretto testa-collo
Uno studio prospettico conferma le evidenze di efficacia e sicurezza dell’adroterapia con ioni carbonio nel controllo dei carcinomi adenoideo-cistici e di altre forme non squamose del distretto testa-collo, con esiti particolarmente favorevoli in caso di
L’adroterapia con ioni carbonio offre la possibilità di controllare la malattia e migliorare la sopravvivenza di pazienti interessati da carcinomi a cellule non squamose del distretto testa-collo, di norma resistenti alla radioterapia convenzionale con fotoni e ai regimi chemioterapici disponibili. A confermare le precedenti evidenze favorevoli in questo senso è uno studio prospettico condotto su 35 pazienti affetti principalmente da adenocarcinoma adenoideo-cistico (60% dei casi), trattati con ioni carbonio presso il GunmaUniversityHeavyIonMedical Center di Maebashi (Giappone), dopo conferma istologica della neoplasia.
Per essere inclusi nello studio, i pazienti dovevano avere un’età compresa tra 16 e 80 anni, tumore misurabile N0-1 M0 e performance status 0-2, non essere mai stati sottoposti a radioterapia a livello di testa e collo, non aver ricevuto chemioterapia nei 30 giorni precedenti l’arruolamento né presentare infezioni non controllate, tumori in altre sedi o comorbilità severe. L’adroterapia con ioni carbonio è stata somministrata al dosaggio di 64,0 Gy RBE (Relative BiologicalEffectiveness) a 32 pazienti e di 57,6 Gy RBE ai restanti tre, in 16 frazioni in entrambi i casi.
Il trattamento ha permesso di ottenere il controllo locale della malattia a tre anni nel 93% dei pazienti (end point primario dello studio) e una sopravvivenza globale (OS, OverallSurvival) a tre anni nell’88% dei casi (end point secondario), a conferma dell’efficacia degli ioni carbonio nell’aggredire e nel neutralizzare tumori altrimenti difficilmente attaccabili.
Esiti particolarmente incoraggianti sono stati ottenuti nei carcinomi non squamosi di minori dimensioni (T2, 5/35 pazienti) e nei tumori diversi dal carcinoma adenoideo-cistico (tra cui 5 neuroblastomi olfattivi, 4 carcinomi mucoepidermoidi e 2 adenocarcinomi): in entrambi i casi, il controllo locale della malattia a tre anni è stato del 100%.
La minore dimensione del tumore è risultata correlata anche all’OS a tre anni, risultata pari al 100% per i tumori T2, e alla localizzazione della neoplasia. In questo secondo caso, l’OS a tre anni è arrivata al 100% per i carcinomi presenti a livello della cavità orale, della faringe e delle parotidi, all’88% per i tumori del seno mascellare e della cavità nasale.
Ulteriori end point secondari esaminati comprendevano il tasso di sopravvivenza libera da malattia (PFS) a tre anni (risultato globalmente pari al 71% e al 100% nei pazienti con tumore T2), la qualità di vita correlata alla salute (valutata con questionario SF-8, prima e dopo 1, 3, 6, 12 e 24 mesi dall’adroterapia) e gli eventi avversi acuti e tardivi.
Relativamente a quest’ultimo aspetto, il trattamento ha comportato complicanze in una quota non trascurabile di pazienti, con sviluppo di mucosite e dermatite acute radioindotte di grado 2-3 rispettivamente nel 65% e nel 31% dei trattati e di mucosite tardiva radioindotta di grado 2 e 3 rispettivamente in 11 e in 1 pazienti.
Mucosite e dermatite acute sono rapidamente migliorate con terapia conservativa e non sembrano costituire una criticità rilevate. Per ridurre l’incidenza di eventi avversi tardivi si ritiene indispensabile prevedere un’attenta pianificazione iniziale della dose nell’ottica di limitare il disagio per il paziente e tutelarne la qualità di vita, senza inficiare l’efficacia del trattamento con ioni carbonio.
Il tasso di tossicità G3 sia acuta che tardiva rilevata nel seguente studio è nettamente inferiore a quanto segnalato in trattamenti convenzionali (tossicità G3/4 mucosa e cutanea intorno al 50%).
Reference
Shirai K et al. Prospective observational study of carbon-ion radiotherapy for non-squamous cell carcinoma of the head and neck. Cancer Sci 2017; doi:10.1111/cas.13325
|
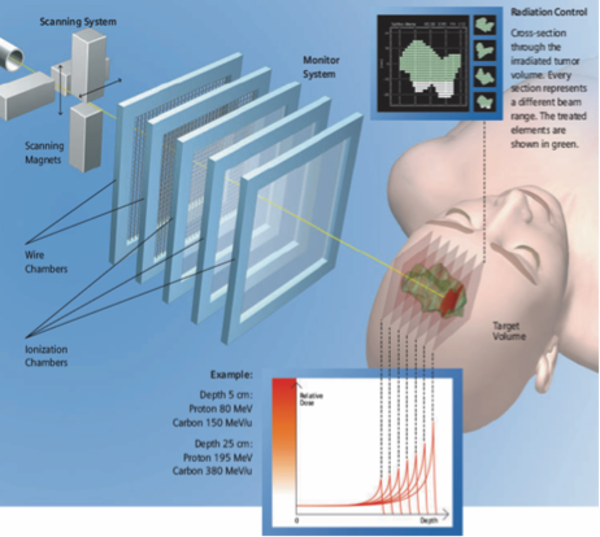 Carcinoma adenoideo-cistico: la dose di ioni carbonio incide sull’outcome
Somministrare un dosaggio sufficientemente elevato di ioni carbonio è cruciale per ottenere un controllo locale ottimale dei carcinomi adenoideo-cistici e un miglioramento della sopravvivenza globale, pur senza incidere sul rischio di metastasi a distanza
Rispetto a quanto osservato dopo chirurgia o radioterapia convenzionale, il controllo locale ottenuto con adroterapia con ioni carbonio (CIRT) dei carcinomi adenoideo-cistici (ACC) del distretto testa-collo appare migliore e indipendente dall’istologia solida o non-solida del tumore, mentre la dose somministrata e il volume della massa tumorale hanno un impatto sulla prognosi. A ciò corrisponde una migliore sopravvivenza anche nei pazienti con forme più aggressive, se trattati con dosaggio sufficiente, ma non una riduzione delle metastasi a distanza, contro le quali dovranno essere individuate strategie specifiche, come per esempio la combinazione di CIRT e immuno/chemioterapia.
Sono queste le conclusioni derivanti dalla valutazione retrospettiva di 100 pazienti con ACC della testa e del collo trattati con ioni carbonio presso il National Institute of RadiologicalSciences - National Institutes for Quantum and RadiologicalSciences and Technology di Chiba (Giappone) tra Dicembre 2006 e Luglio 2013, nel contesto di uno studio finalizzato a individuare i fattori prognostici di controllo locale (LC) e l’impatto del trattamento su sopravvivenza globale (OS, OverallSurvival) e sopravvivenza libera da metastasi a distanza (DMFS, DistantMetastatis Free Survival).
Dei pazienti considerati (età media 57 anni, 65% donne), il 61% presentava un tumore esteso (T4), con un volume tumorale lordo (GTV) mediano di 38,6 ml, precedentemente trattato chirurgicamente nel 15% dei casi; la maggior parte dei pazienti non presentava coinvolgimento linfonodale (N0 94%) e nessuno era interessato da metastasi all’arruolamento (M0 100%); nel 17% dei casi l’ACC era caratterizzato da una componente solida e le localizzazioni prevalenti del tumore comprendevano il naso o i seni paranasali (50% dei casi) oppure il cavo orale, la faringe o le ghiandole salivari (42% dei casi). Un terzo dei pazienti (n=33) è stato trattato con CIRT al dosaggio di 57,6 Gy RBE (Relative BiologicalEffectiveness), mentre i restanti 67 hanno ricevuto 64,0 Gy RBE, in entrambi i casi in 16 frazioni nell’arco di 4 settimane.
Durante un follow-up mediano di 60 mesi (range 6-116 mesi), 32 pazienti hanno sviluppato recidive locali e un paziente ha sviluppato una metastasi in un linfonodo cervicale, mentre in 30 pazienti sono state riscontrate metastasi a distanza, localizzate principalmente a livello di polmoni (70%), ossa (17%) e fegato (6%).
Il LC, l’OS e la DMFS a 5 anni nell’intero campione sono risultati pari a 68,6%, 74,8% e 65,7%. Analizzando i tre parametri in funzione del dosaggio di ioni carbonio somministrato, è stato osservato che l’istologia solida aveva un impatto sul LC a 5 anni esclusivamente tra i pazienti trattati al minor dosaggio (0% vs 53,4%; p=0,001), mentre perdeva significato prognostico quando i pazienti ricevevano una dose sufficientemente elevata (83,3% vs 83,0%; p=0,210). Dose inferiore (HR 3,77) e GTV maggiore (HR 3,36) si sono confermati fattori prognostici negativi nell’ambito dell’analisi multivariata.
Relativamente all’OS a 5 anni, l’analisi uni-variata ha indicato che le dimensioni del tumore (T), il sottotipo istologico e il GTV erano in grado di influenzare significativamente la prognosi. GTV (HR 3,63) e istologia solida (HR 2,43) si sono confermati fattori prognostici anche nell’analisi multi-variata. In particolare, l’OS a 5 anni è risultata pari al 41,2% nelle forme solide vs 81,2% delle forme non-solide.
Coinvolgimento linfonodale (N >0), GTV e istologia solida sono risultati prognostici anche per la DMFS a 5 anni, sia nell’analisi uni-variata sia in quella multivariata. In particolare, le DMFS a 5 anni tra i pazienti con forme a istologia solida vs non-solida sono risultate pari al 29,7% vs 72,8%.
Come sottolineato dagli Autori, questi risultati, oltre a confermare l’efficacia della CIRT nella gestione di tumori aggressivi e difficili da controllare con gli altri approcci terapeutici disponibili, permettono di attuare una migliore selezione dei pazienti da trattare e di aggirare le criticità legate alla difficoltà di classificare con precisione l’istologia degli ACC della testa e del collo (spesso caratterizzati da istologia mista).
Per analoghi pazienti, affetti da neoplasie avanzate trattate con radiazioni convenzionali, il controllo locale di malattia a cinque anni varia dal 36 al 43% a seconda delle casistiche.
Reference
Ikawa H et al. Prognostic factors of adenoid cystic carcinoma of the head and neck in carbon-ion radiotherapy: The impact of histological subtypes. RadiotherOncol 2017;123(3):387-393; doi:10.1016/j.radonc.2017.04.026
Carcinoma adenoideo-cistico: la dose di ioni carbonio incide sull’outcome
Somministrare un dosaggio sufficientemente elevato di ioni carbonio è cruciale per ottenere un controllo locale ottimale dei carcinomi adenoideo-cistici e un miglioramento della sopravvivenza globale, pur senza incidere sul rischio di metastasi a distanza
Rispetto a quanto osservato dopo chirurgia o radioterapia convenzionale, il controllo locale ottenuto con adroterapia con ioni carbonio (CIRT) dei carcinomi adenoideo-cistici (ACC) del distretto testa-collo appare migliore e indipendente dall’istologia solida o non-solida del tumore, mentre la dose somministrata e il volume della massa tumorale hanno un impatto sulla prognosi. A ciò corrisponde una migliore sopravvivenza anche nei pazienti con forme più aggressive, se trattati con dosaggio sufficiente, ma non una riduzione delle metastasi a distanza, contro le quali dovranno essere individuate strategie specifiche, come per esempio la combinazione di CIRT e immuno/chemioterapia.
Sono queste le conclusioni derivanti dalla valutazione retrospettiva di 100 pazienti con ACC della testa e del collo trattati con ioni carbonio presso il National Institute of RadiologicalSciences - National Institutes for Quantum and RadiologicalSciences and Technology di Chiba (Giappone) tra Dicembre 2006 e Luglio 2013, nel contesto di uno studio finalizzato a individuare i fattori prognostici di controllo locale (LC) e l’impatto del trattamento su sopravvivenza globale (OS, OverallSurvival) e sopravvivenza libera da metastasi a distanza (DMFS, DistantMetastatis Free Survival).
Dei pazienti considerati (età media 57 anni, 65% donne), il 61% presentava un tumore esteso (T4), con un volume tumorale lordo (GTV) mediano di 38,6 ml, precedentemente trattato chirurgicamente nel 15% dei casi; la maggior parte dei pazienti non presentava coinvolgimento linfonodale (N0 94%) e nessuno era interessato da metastasi all’arruolamento (M0 100%); nel 17% dei casi l’ACC era caratterizzato da una componente solida e le localizzazioni prevalenti del tumore comprendevano il naso o i seni paranasali (50% dei casi) oppure il cavo orale, la faringe o le ghiandole salivari (42% dei casi). Un terzo dei pazienti (n=33) è stato trattato con CIRT al dosaggio di 57,6 Gy RBE (Relative BiologicalEffectiveness), mentre i restanti 67 hanno ricevuto 64,0 Gy RBE, in entrambi i casi in 16 frazioni nell’arco di 4 settimane.
Durante un follow-up mediano di 60 mesi (range 6-116 mesi), 32 pazienti hanno sviluppato recidive locali e un paziente ha sviluppato una metastasi in un linfonodo cervicale, mentre in 30 pazienti sono state riscontrate metastasi a distanza, localizzate principalmente a livello di polmoni (70%), ossa (17%) e fegato (6%).
Il LC, l’OS e la DMFS a 5 anni nell’intero campione sono risultati pari a 68,6%, 74,8% e 65,7%. Analizzando i tre parametri in funzione del dosaggio di ioni carbonio somministrato, è stato osservato che l’istologia solida aveva un impatto sul LC a 5 anni esclusivamente tra i pazienti trattati al minor dosaggio (0% vs 53,4%; p=0,001), mentre perdeva significato prognostico quando i pazienti ricevevano una dose sufficientemente elevata (83,3% vs 83,0%; p=0,210). Dose inferiore (HR 3,77) e GTV maggiore (HR 3,36) si sono confermati fattori prognostici negativi nell’ambito dell’analisi multivariata.
Relativamente all’OS a 5 anni, l’analisi uni-variata ha indicato che le dimensioni del tumore (T), il sottotipo istologico e il GTV erano in grado di influenzare significativamente la prognosi. GTV (HR 3,63) e istologia solida (HR 2,43) si sono confermati fattori prognostici anche nell’analisi multi-variata. In particolare, l’OS a 5 anni è risultata pari al 41,2% nelle forme solide vs 81,2% delle forme non-solide.
Coinvolgimento linfonodale (N >0), GTV e istologia solida sono risultati prognostici anche per la DMFS a 5 anni, sia nell’analisi uni-variata sia in quella multivariata. In particolare, le DMFS a 5 anni tra i pazienti con forme a istologia solida vs non-solida sono risultate pari al 29,7% vs 72,8%.
Come sottolineato dagli Autori, questi risultati, oltre a confermare l’efficacia della CIRT nella gestione di tumori aggressivi e difficili da controllare con gli altri approcci terapeutici disponibili, permettono di attuare una migliore selezione dei pazienti da trattare e di aggirare le criticità legate alla difficoltà di classificare con precisione l’istologia degli ACC della testa e del collo (spesso caratterizzati da istologia mista).
Per analoghi pazienti, affetti da neoplasie avanzate trattate con radiazioni convenzionali, il controllo locale di malattia a cinque anni varia dal 36 al 43% a seconda delle casistiche.
Reference
Ikawa H et al. Prognostic factors of adenoid cystic carcinoma of the head and neck in carbon-ion radiotherapy: The impact of histological subtypes. RadiotherOncol 2017;123(3):387-393; doi:10.1016/j.radonc.2017.04.026
|
 La terapia con protoni sugli organi in movimento: l'esperienza di CNAO
L’utilizzo delle tecniche di adroterapia 4D per l’irradiazione con adroni di organi in movimento rappresentano un’importante sfida tecnologica e metodologica, particolarmente efficace per il trattamento selettivo di gravi forme di tumore al pancreas, al f
L’implementazione di una tecnica di irradiazione con adroni di organi in movimento rappresenta una sfida tecnologica e metodologica di grande interesse nella comunità scientifico-clinica internazionale. Il concetto risiede nella realizzazione di una tecnica di irraggiamento sincronizzata ai movimenti dovuti alla respirazione di tumori mobili. Questa tecnica, denominata adroterapia-4D, risulta particolarmente efficace per il trattamento selettivo di gravi forme di tumore quali il tumore al pancreas, al fegato, al polmone. Considerando la predisposizione dei sistemi di delivery della dose con scanning attivo di poter essere rapidamente indirizzati verso target in movimento, il problema principale risiede nella capacità di localizzare in tempo reale la posizione del target e degli organi critici circostanti e di fornire questa informazione con ritardo trascurabile ai magneti di scansione del fascio (in-plane tracking) e ad un sistema dedicato di modulazione dell’energia del fascio (in-depth tracking). Tecniche di tumor tracking sono già disponibili nella radioterapia tradizionale e si basano su modelli di correlazione esterno-interno che prevedono una fase di addestramento del modello di correlazione nella fase immediatamente precedente l’irradiazione, finalizzata a stimare i parametri ottimi della correlazione su base paziente specifica. A valle di questa sorta di addestramento, la localizzazione del target viene stimata a partire dall’informazione proveniente dai sistemi di localizzazione dei surrogati esterni (sistemi di computer vision basati su tecniche di tracking all’infrarosso) che, data in pasto al modello di correlazione, stima la posizione del target con elevata risoluzione temporale.
La fattibilità tecnologica di questa tecnica è stata già investigata e provata recentemente aprendo la strada alla fase successiva finalizzata all’implementazione clinica della stessa. Tuttavia, questo passaggio risulta particolarmente complesso e delicato, a causa della elevata sensibilità dei fasci di particelle cariche a variazioni di densità dei tessuti attraversati lungo il loro cammino verso il bersaglio. Questo impone strategie specifiche di pianificazione del trattamento basate su imaging risolto in tempo (TAC e Risonanza Magnetica in 4D), la generazione di modelli di movimento paziente-specifici con metodi di registrazione di immagini con deformazione, l’ impiego combinato durante il trattamento di sistemi di visione artificiale con telecamere agli infrarossi e di dispositivi di verifica a raggi-X.
La ricerca ha consentito per ora di ottenere risultati positivi in simulazione e in esperimenti di adroterapia-4D con tumour tracking su fantocci antropomorfi radioequivalenti, anche nel quadro di progetti europei (Progetto ULICE) (Seregni et al., PMB, 2013; Fattori et al., TCRT, 2014). L’obiettivo è ora quello di coagulare le competenze multidisciplinari necessarie a livello nazionale ed internazionale, per rendere questa tecnica applicabile sui pazienti in modo sicuro ed efficace.
Il trattamento con gating respiratorio
Se l’adroterapia 4D con tumor tracking è ancora in fase di studio e sviluppo, metodi di irraggiamento con adroni correlati alla respirazione sono già implementati clinicamente. Il più diffuso, applicato anche presso il CNAO, è il cosiddetto trattamento con gating respiratorio (Ciocca et al, Phys Med, 2016). La metodica prevede di inviare il fascio di terapia al paziente solo in corrispondenza di una specifica fase del ciclo respiratorio, definita in fase di pianificazione del trattamento sulla base di una TAC-4D, e individuata in linea da sistemi installati nel bunker di terapia che misurano l’attività respiratoria del paziente già posizionato per la terapia. La combinazione di questa modalità di irradiazione intermittente, sincronizzata al respiro, con opportuni sistemi di contenimento dell’escursione respiratoria (maschere di immobilizzazione) e tecniche di rescanning del fascio (la dose viene rilasciata in vari passaggi per limitare le incertezze dovute al movimento respiratorio residuo nella fase respiratoria di irradiazione), è possibile ottenere un’accuratezza geometrica sufficiente per garantire un’ottima distribuzione della dose secondo quanto indicato nel piano di trattamento. Fondamentale è in questo caso assicurare la regolarità del pattern respiratorio del paziente e ricorrere a sistemi ridondanti (tracking ottico, fasce addominali sensorizzate con sensori di pressione) per combinare i segnali relativi all’attività respiratoria, abilitando l’erogazione del fascio solo in presenza di una via libera da parte di tutti i sistemi messi in opera.
In ogni caso, le tecniche di irradiazione risolte in tempo (4D) richiedono l’impiego di protocolli di Quality Assurance, volti a verificare l’effettiva corretta deposizione della dose secondo quanto pianificato. In questo senso vengono in aiuto metodi basati su modelli di movimento (estratti dalla TAC -4D ) di pianificazione, che sulla base del segnale legato all’attività sono in grado di stimare l’intera configurazione anatomica del paziente istante per istante con particolare riferimento al canale di ingresso del fascio (Fassi et al., PMB, 2015; Meschini et al., Phys Med, 2017; Wölfelschneider et al., Med Phys, 2017). Anche tecniche di dosimetria in-vivo basate su PET -4D sono proposte come metodo di verifica in linea della qualità della somministrazione della dose correlata alla respirazione e ampiamente studiate in CNAO in collaborazione con centri di ricerca clinica europei (De Bernardi et al., Med Phys, 2016; Gianoli et al., PMB, 2016; Bisogni et al., J Med Imaging, 2017)
References
Ciocca M, Mirandola A, Molinelli S, Russo S, Mastella E, Vai A, Mairani A, Magro G, Pella A, Donetti M, Valvo F, Fossati P, Baroni G. Commissioning of the 4-D treatment delivery system for organ motion management in synchrotron-based scanning ion beams. Phys Med. 2016 Dec; 32(12):1667-1671. doi: 10.1016/j.ejmp.2016.11.107. Epub 2016 Nov 24
Wölfelschneider J, Seregni M, Fassi A, Ziegler M, Baroni G, Fietkau R, Riboldi M, Bert C. Examination of a deformable motion model for respiratory movements and 4D dose calculations using different driving surrogates. Med Phys. 2017 Jun; 44(6):2066-2076. doi: 10.1002/mp.12243. Epub 2017 May 12.
Meschini G, Seregni M, Pella A, Ciocca M, Fossati P, Valvo F, Riboldi M, Baroni G. Evaluation of residual abdominal tumour motion in carbon ion gated treatments through respiratory motion modelling. Phys Med. 2017 Feb;34:28-37. doi: 10.1016/j.ejmp.2017.01.009. Epub 2017 Jan 18.
Bisogni MG, Attili A, Battistoni G, Belcari N, Camarlinghi N, Cerello P, Coli S, Del Guerra A, Ferrari A, Ferrero V, Fiorina E, Giraudo G, Kostara E, Morrocchi M, Pennazio F, Peroni C, Piliero MA, Pirrone G, Rivetti A, Rolo MD, Rosso V, Sala P, Sportelli G, Wheadon R. J Med Imaging (Bellingham). 2017 Jan;4(1):011005. Epub 2016 Dec 2.
Gianoli C, Kurz C, Riboldi M, Bauer J, Fontana G, Baroni G, Debus J, Parodi K. Clinical evaluation of 4D PET motion compensation strategies for treatment verification in ion beam therapy. Phys Med Biol. 2016 Jun 7; 61(11):4141-55. doi: 10.1088/0031-9155/61/11/4141. Epub 2016 May 18.
De Bernardi E, Ricotti R, Riboldi M, Baroni G, Parodi K, Gianoli C. 4D ML reconstruction as a tool for volumetric PET-based treatment verification in ion beam radiotherapy. Med Phys. 2016 Feb; 43(2):710-26. doi: 10.1118/1.4939227.
Fassi A, Seregni M, Riboldi M, Cerveri P, Sarrut D, Ivaldi GB, de Fatis PT, Liotta M, Baroni G. Surrogate-driven deformable motion model for organ motion tracking in particle radiation therapy. Phys Med Biol. 2015 Feb 21; 60(4):1565-82. doi: 10.1088/0031-9155/60/4/1565. Epub 2015 Jan 23.
Fattori G, Saito N, Seregni M, Kaderka R, Pella A, Constantinescu A, Riboldi M, Steidl P, Cerveri P, Bert C, Durante M, Baroni G. Commissioning of an integrated platform for time-resolved treatment delivery in scanned ion beam therapy by means of optical motion monitoring. Technol Cancer Res Treat. 2014 Dec;13(6):517-28. doi: 10.7785/tcrtexpress.2013.600275. Epub 2013 Dec 17.
Seregni M, Kaderka R, Fattori G, Riboldi M, Pella A, Constantinescu A, Saito N, Durante M, Cerveri P, Bert C, Baroni G. Tumor tracking based on correlation models in scanned ion beam therapy: an experimental study. Phys Med Biol. 2013 Jul 7;58(13):4659-78. doi: 10.1088/0031-9155/58/13/4659. Epub 2013 Jun 18.
�
UN CASO CLINICO
Si riporta il caso clinico di un uomo di 63 anni arrivato al CNAO a seguito di una diagnosi di carcinoma del fegato. Di seguito sono descritti i passaggi del percorso diagnostico terapeutico cui si è sottoposto.
IL DECORSO PRE-CNAO
2013: trapianto ortotopico di fegato per cirrosi HCV correlata (riscontro all’esame istologico definitivo del fegato nativo di HCC). Segue terapia antivirale con Interferon e Ribavirina da novembre 2008 a novembre 2009 (non responder) per recidiva epatitica istologicamente accertata HCV relata.
In seguito ad incremento dell’alfa-feto proteina (AFP) il paziente ha dovuto eseguire numerosi esami:
• Ecografia con mdc: si conferma la presenza di nodulo di HCC paracavale, all’emergenza della vena sovra epatica sinistra, di 16 mm di diametro massimo.
• Radiofrequenza percutanea della lesione nodulare.
• RM addome: esiti di radiofrequenza su S8 in sede paracavale. Non si osservano segni di persistenza o di recidiva di malattia a tale livello.
• Ecografia dell’addome: in sede paracavale a ridosso della vena sovra epatica di sinistra, nella sede della pregressa termo ablazione percutanea mediante RF, si osserva lieve disomogeneità strutturale del diametro di 17 mm compatibile con area necrotica.
• TAC con mdc: con prevalente sviluppo interepatodiaframmatica posteriore si osserva una lesione espansiva di morfologia ovalare, del massimo diametro di 5.5 x 1.5 cm, riferibile a recidiva di malattia. La lesione appare indissociabile dalla vena cava di cui oltrepassa la parete per una lunghezza di almeno 18 mm, producendo al suo interno un piccolo trombo neoplastico sviluppato al suo interno sino a circa 18 mm di lunghezza, ma privo di significato emodinamico.
In considerazione delle dimensioni della lesione della infiltrazione dei vasi viene proposto per trattamento con ioni carbonio.
IL TRATTAMENTO RADIANTE CON ADRONI
Dal 01.09.2014 al 18.09.2014 è stato effettuato un trattamento radiante con ioni carbonio con sistema di scanning attivo per una dose totale 55,2 di Gy(RBE) (4,6 Gy(RBE)/frazione, 12 frazioni, 4 frazioni/settimana), con tecnica IMPT (Intensity Modulated Particle Therapy).
Il decorso clinico ha dimostrato un’ottima tolleranza al trattamento e non è stata registrata nessuna tossicità.
IL FOLLOW-UP: (FUP 37mesi)
Il paziente è attualmente in controllo locale di malattia senza alcuna tossicità correlata al trattamento. Nell’ottobre 2017 ha effettuato una RM addome superiore: rispetto al precedente controllo, appare ridotta in dimensioni, con margini sfumati e mal definiti la nota lesione trattata in cupola epatica in adiacenza alla confluenza delle vene sovraepatiche in VCI. Non si apprezzano aree focali di iperenhancement in fase arteriosa sospette per nuovi noduli di HCC. Non sicuramente più distinguibile l’immagine pseudo-nodulare ipovascolare segnalata al VI segmento. Invariati i restanti reperti.
La terapia con protoni sugli organi in movimento: l'esperienza di CNAO
L’utilizzo delle tecniche di adroterapia 4D per l’irradiazione con adroni di organi in movimento rappresentano un’importante sfida tecnologica e metodologica, particolarmente efficace per il trattamento selettivo di gravi forme di tumore al pancreas, al f
L’implementazione di una tecnica di irradiazione con adroni di organi in movimento rappresenta una sfida tecnologica e metodologica di grande interesse nella comunità scientifico-clinica internazionale. Il concetto risiede nella realizzazione di una tecnica di irraggiamento sincronizzata ai movimenti dovuti alla respirazione di tumori mobili. Questa tecnica, denominata adroterapia-4D, risulta particolarmente efficace per il trattamento selettivo di gravi forme di tumore quali il tumore al pancreas, al fegato, al polmone. Considerando la predisposizione dei sistemi di delivery della dose con scanning attivo di poter essere rapidamente indirizzati verso target in movimento, il problema principale risiede nella capacità di localizzare in tempo reale la posizione del target e degli organi critici circostanti e di fornire questa informazione con ritardo trascurabile ai magneti di scansione del fascio (in-plane tracking) e ad un sistema dedicato di modulazione dell’energia del fascio (in-depth tracking). Tecniche di tumor tracking sono già disponibili nella radioterapia tradizionale e si basano su modelli di correlazione esterno-interno che prevedono una fase di addestramento del modello di correlazione nella fase immediatamente precedente l’irradiazione, finalizzata a stimare i parametri ottimi della correlazione su base paziente specifica. A valle di questa sorta di addestramento, la localizzazione del target viene stimata a partire dall’informazione proveniente dai sistemi di localizzazione dei surrogati esterni (sistemi di computer vision basati su tecniche di tracking all’infrarosso) che, data in pasto al modello di correlazione, stima la posizione del target con elevata risoluzione temporale.
La fattibilità tecnologica di questa tecnica è stata già investigata e provata recentemente aprendo la strada alla fase successiva finalizzata all’implementazione clinica della stessa. Tuttavia, questo passaggio risulta particolarmente complesso e delicato, a causa della elevata sensibilità dei fasci di particelle cariche a variazioni di densità dei tessuti attraversati lungo il loro cammino verso il bersaglio. Questo impone strategie specifiche di pianificazione del trattamento basate su imaging risolto in tempo (TAC e Risonanza Magnetica in 4D), la generazione di modelli di movimento paziente-specifici con metodi di registrazione di immagini con deformazione, l’ impiego combinato durante il trattamento di sistemi di visione artificiale con telecamere agli infrarossi e di dispositivi di verifica a raggi-X.
La ricerca ha consentito per ora di ottenere risultati positivi in simulazione e in esperimenti di adroterapia-4D con tumour tracking su fantocci antropomorfi radioequivalenti, anche nel quadro di progetti europei (Progetto ULICE) (Seregni et al., PMB, 2013; Fattori et al., TCRT, 2014). L’obiettivo è ora quello di coagulare le competenze multidisciplinari necessarie a livello nazionale ed internazionale, per rendere questa tecnica applicabile sui pazienti in modo sicuro ed efficace.
Il trattamento con gating respiratorio
Se l’adroterapia 4D con tumor tracking è ancora in fase di studio e sviluppo, metodi di irraggiamento con adroni correlati alla respirazione sono già implementati clinicamente. Il più diffuso, applicato anche presso il CNAO, è il cosiddetto trattamento con gating respiratorio (Ciocca et al, Phys Med, 2016). La metodica prevede di inviare il fascio di terapia al paziente solo in corrispondenza di una specifica fase del ciclo respiratorio, definita in fase di pianificazione del trattamento sulla base di una TAC-4D, e individuata in linea da sistemi installati nel bunker di terapia che misurano l’attività respiratoria del paziente già posizionato per la terapia. La combinazione di questa modalità di irradiazione intermittente, sincronizzata al respiro, con opportuni sistemi di contenimento dell’escursione respiratoria (maschere di immobilizzazione) e tecniche di rescanning del fascio (la dose viene rilasciata in vari passaggi per limitare le incertezze dovute al movimento respiratorio residuo nella fase respiratoria di irradiazione), è possibile ottenere un’accuratezza geometrica sufficiente per garantire un’ottima distribuzione della dose secondo quanto indicato nel piano di trattamento. Fondamentale è in questo caso assicurare la regolarità del pattern respiratorio del paziente e ricorrere a sistemi ridondanti (tracking ottico, fasce addominali sensorizzate con sensori di pressione) per combinare i segnali relativi all’attività respiratoria, abilitando l’erogazione del fascio solo in presenza di una via libera da parte di tutti i sistemi messi in opera.
In ogni caso, le tecniche di irradiazione risolte in tempo (4D) richiedono l’impiego di protocolli di Quality Assurance, volti a verificare l’effettiva corretta deposizione della dose secondo quanto pianificato. In questo senso vengono in aiuto metodi basati su modelli di movimento (estratti dalla TAC -4D ) di pianificazione, che sulla base del segnale legato all’attività sono in grado di stimare l’intera configurazione anatomica del paziente istante per istante con particolare riferimento al canale di ingresso del fascio (Fassi et al., PMB, 2015; Meschini et al., Phys Med, 2017; Wölfelschneider et al., Med Phys, 2017). Anche tecniche di dosimetria in-vivo basate su PET -4D sono proposte come metodo di verifica in linea della qualità della somministrazione della dose correlata alla respirazione e ampiamente studiate in CNAO in collaborazione con centri di ricerca clinica europei (De Bernardi et al., Med Phys, 2016; Gianoli et al., PMB, 2016; Bisogni et al., J Med Imaging, 2017)
References
Ciocca M, Mirandola A, Molinelli S, Russo S, Mastella E, Vai A, Mairani A, Magro G, Pella A, Donetti M, Valvo F, Fossati P, Baroni G. Commissioning of the 4-D treatment delivery system for organ motion management in synchrotron-based scanning ion beams. Phys Med. 2016 Dec; 32(12):1667-1671. doi: 10.1016/j.ejmp.2016.11.107. Epub 2016 Nov 24
Wölfelschneider J, Seregni M, Fassi A, Ziegler M, Baroni G, Fietkau R, Riboldi M, Bert C. Examination of a deformable motion model for respiratory movements and 4D dose calculations using different driving surrogates. Med Phys. 2017 Jun; 44(6):2066-2076. doi: 10.1002/mp.12243. Epub 2017 May 12.
Meschini G, Seregni M, Pella A, Ciocca M, Fossati P, Valvo F, Riboldi M, Baroni G. Evaluation of residual abdominal tumour motion in carbon ion gated treatments through respiratory motion modelling. Phys Med. 2017 Feb;34:28-37. doi: 10.1016/j.ejmp.2017.01.009. Epub 2017 Jan 18.
Bisogni MG, Attili A, Battistoni G, Belcari N, Camarlinghi N, Cerello P, Coli S, Del Guerra A, Ferrari A, Ferrero V, Fiorina E, Giraudo G, Kostara E, Morrocchi M, Pennazio F, Peroni C, Piliero MA, Pirrone G, Rivetti A, Rolo MD, Rosso V, Sala P, Sportelli G, Wheadon R. J Med Imaging (Bellingham). 2017 Jan;4(1):011005. Epub 2016 Dec 2.
Gianoli C, Kurz C, Riboldi M, Bauer J, Fontana G, Baroni G, Debus J, Parodi K. Clinical evaluation of 4D PET motion compensation strategies for treatment verification in ion beam therapy. Phys Med Biol. 2016 Jun 7; 61(11):4141-55. doi: 10.1088/0031-9155/61/11/4141. Epub 2016 May 18.
De Bernardi E, Ricotti R, Riboldi M, Baroni G, Parodi K, Gianoli C. 4D ML reconstruction as a tool for volumetric PET-based treatment verification in ion beam radiotherapy. Med Phys. 2016 Feb; 43(2):710-26. doi: 10.1118/1.4939227.
Fassi A, Seregni M, Riboldi M, Cerveri P, Sarrut D, Ivaldi GB, de Fatis PT, Liotta M, Baroni G. Surrogate-driven deformable motion model for organ motion tracking in particle radiation therapy. Phys Med Biol. 2015 Feb 21; 60(4):1565-82. doi: 10.1088/0031-9155/60/4/1565. Epub 2015 Jan 23.
Fattori G, Saito N, Seregni M, Kaderka R, Pella A, Constantinescu A, Riboldi M, Steidl P, Cerveri P, Bert C, Durante M, Baroni G. Commissioning of an integrated platform for time-resolved treatment delivery in scanned ion beam therapy by means of optical motion monitoring. Technol Cancer Res Treat. 2014 Dec;13(6):517-28. doi: 10.7785/tcrtexpress.2013.600275. Epub 2013 Dec 17.
Seregni M, Kaderka R, Fattori G, Riboldi M, Pella A, Constantinescu A, Saito N, Durante M, Cerveri P, Bert C, Baroni G. Tumor tracking based on correlation models in scanned ion beam therapy: an experimental study. Phys Med Biol. 2013 Jul 7;58(13):4659-78. doi: 10.1088/0031-9155/58/13/4659. Epub 2013 Jun 18.
�
UN CASO CLINICO
Si riporta il caso clinico di un uomo di 63 anni arrivato al CNAO a seguito di una diagnosi di carcinoma del fegato. Di seguito sono descritti i passaggi del percorso diagnostico terapeutico cui si è sottoposto.
IL DECORSO PRE-CNAO
2013: trapianto ortotopico di fegato per cirrosi HCV correlata (riscontro all’esame istologico definitivo del fegato nativo di HCC). Segue terapia antivirale con Interferon e Ribavirina da novembre 2008 a novembre 2009 (non responder) per recidiva epatitica istologicamente accertata HCV relata.
In seguito ad incremento dell’alfa-feto proteina (AFP) il paziente ha dovuto eseguire numerosi esami:
• Ecografia con mdc: si conferma la presenza di nodulo di HCC paracavale, all’emergenza della vena sovra epatica sinistra, di 16 mm di diametro massimo.
• Radiofrequenza percutanea della lesione nodulare.
• RM addome: esiti di radiofrequenza su S8 in sede paracavale. Non si osservano segni di persistenza o di recidiva di malattia a tale livello.
• Ecografia dell’addome: in sede paracavale a ridosso della vena sovra epatica di sinistra, nella sede della pregressa termo ablazione percutanea mediante RF, si osserva lieve disomogeneità strutturale del diametro di 17 mm compatibile con area necrotica.
• TAC con mdc: con prevalente sviluppo interepatodiaframmatica posteriore si osserva una lesione espansiva di morfologia ovalare, del massimo diametro di 5.5 x 1.5 cm, riferibile a recidiva di malattia. La lesione appare indissociabile dalla vena cava di cui oltrepassa la parete per una lunghezza di almeno 18 mm, producendo al suo interno un piccolo trombo neoplastico sviluppato al suo interno sino a circa 18 mm di lunghezza, ma privo di significato emodinamico.
In considerazione delle dimensioni della lesione della infiltrazione dei vasi viene proposto per trattamento con ioni carbonio.
IL TRATTAMENTO RADIANTE CON ADRONI
Dal 01.09.2014 al 18.09.2014 è stato effettuato un trattamento radiante con ioni carbonio con sistema di scanning attivo per una dose totale 55,2 di Gy(RBE) (4,6 Gy(RBE)/frazione, 12 frazioni, 4 frazioni/settimana), con tecnica IMPT (Intensity Modulated Particle Therapy).
Il decorso clinico ha dimostrato un’ottima tolleranza al trattamento e non è stata registrata nessuna tossicità.
IL FOLLOW-UP: (FUP 37mesi)
Il paziente è attualmente in controllo locale di malattia senza alcuna tossicità correlata al trattamento. Nell’ottobre 2017 ha effettuato una RM addome superiore: rispetto al precedente controllo, appare ridotta in dimensioni, con margini sfumati e mal definiti la nota lesione trattata in cupola epatica in adiacenza alla confluenza delle vene sovraepatiche in VCI. Non si apprezzano aree focali di iperenhancement in fase arteriosa sospette per nuovi noduli di HCC. Non sicuramente più distinguibile l’immagine pseudo-nodulare ipovascolare segnalata al VI segmento. Invariati i restanti reperti.
|
|
Gentile utente, ricevi questa newsletter a scopo di informazione scientifica a fronte della tua registrazione a CNAO Clinical News sul nostro sito
https://fondazionecnao.it/area-medici,
nella sezione area riservata, oppure perché il tuo indirizzo è stato reso pubblico dall'ente che lo gestisce.
Nel caso in cui non volessi più ricevere la nostra newsletter, clicca qui e sarai indirizzato al link per la cancellazione dell'indirizzo dal nostro database.
Per ulteriori informazioni, puoi collegarti alla pagina https://fondazionecnao.it/privacy-policy
|
|
Clicca qui se non desideri più ricevere la nostra newsletter
|
|




